El amoniaco (NH3) es un gas incoloro, de olor característico y muy corrosivo, usado de manera masiva en la actualidad para la producción de fertilizantes que, a su vez, son necesarios para satisfacer la demanda global de alimentos.
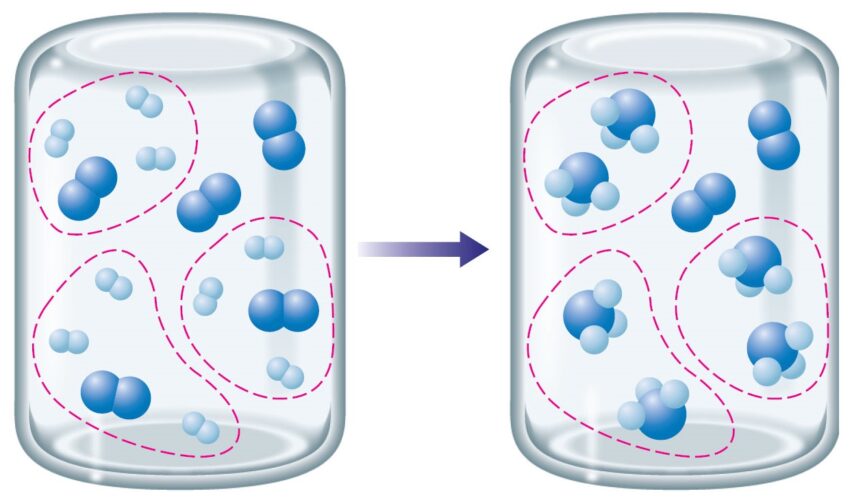
El nitrógeno es un elemento esencial para los organismos vivos porque forma parte de moléculas vitales como los aminoácidos. Y aunque el gas más abundante en el aire es el nitrógeno molecular (N2), este debe ser convertido en amoniaco para poder incorporarse a la biósfera. Hasta hace poco más de 100 años, esta transformación sólo podía realizarse por algunas bacterias a través de un proceso llamado fijación del nitrógeno. Sin embargo, a principios del siglo XX el químico alemán Fritz Haber desarrolló un proceso en el laboratorio para obtener amoniaco a partir de nitrógeno e hidrógeno (H2) moleculares, utilizando un catalizador de hierro a alta presión y temperatura. A su vez, otro químico e ingeniero alemán, llamado Carl Bosch, escaló dicho proceso a nivel industrial para su comercialización. El impacto de estas contribuciones a la sociedad fue tan grande que ambos científicos ganaron el Premio Nobel de Química en 1918 y 1931, respectivamente.
Antes del proceso Bosch-Haber, los fertilizantes se obtenían de fuentes naturales como el guano y salitre, las cuales comenzaban a ser insuficientes para satisfacer la demanda de producción de alimentos en el mundo. Sin embargo, la posibilidad de generar amoniaco de manera artificial revolucionó la industria agraria mundial al disponer de fertilizantes sintéticos, y provocó un aumento dramático en su productividad, por lo que se le considera parcialmente responsable del rápido aumento de la población en el siglo XX.
Adicionalmente a su uso en la agricultura, el amoniaco es una importante materia prima para la producción de plásticos, textiles, colorantes y explosivos. El amoniaco también es un ingrediente común en diversos productos de limpieza domésticos e industriales. Debido a su uso generalizado y masivo a nivel global, su liberación al medio ambiente (al suelo, al agua y al aire) ha ido en aumento, con consecuencias negativas para la salud del ser humano y los ecosistemas.
En particular, las emisiones de amoniaco al aire ocurren principalmente debido a la evaporación de fertilizantes durante la producción de alimentos para el consumo humano y animal. Los desechos de animales en la industria ganadera (orina y estiércol) también generan amoniaco al descomponerse. Otras fuentes que emiten amoniaco al aire son las emisiones vehiculares (producto secundario de los convertidores catalíticos), algunos procesos industriales, y el almacenamiento y tratamiento de desechos.
Aunque el amoniaco puede ser un gas tóxico al ser inhalado, generalmente se encuentra en el aire en concentraciones que no causan daño a la salud; sin embargo, puede reaccionar con otros contaminantes para producir pequeñas partículas suspendidas en el aire, conocidas como PM2.5 por sus siglas en inglés (particulate matter) y por su tamaño menor a 2.5 micras. Al ser inhaladas, estas partículas pueden llegar hasta los alveolos pulmonares y causar inflamación; incluso, pueden entrar al torrente sanguíneo generando efectos negativos a la salud a largo plazo, como problemas cardiovasculares y enfermedades pulmonares. Por ello, es importante determinar, cuantificar y regular los procesos que generan PM2.5.
Históricamente, se ha considerado que las fuentes de PM2.5 más importantes son la emisión del dióxido de azufre (SO2), por la quema de combustibles industriales, y de óxidos de nitrógeno (NO y NO2) por la quema de combustibles vehiculares. Dichos gases se oxidan en la atmósfera para formar ácidos nítrico y sulfúrico, que son algunos de los principales componentes de las partículas. Debido a que algunos de los controles de la contaminación del aire se han dirigido a la regulación de dichos compuestos, su concentración en el aire se ha reducido en los últimos 20 años. Al mismo tiempo, las emisiones de amoniaco han aumentado y permanecen sin ser reguladas, por lo que su importancia como precursor de partículas ha aumentado y son un foco importante de atención de científicos y tomadores de decisiones en la actualidad.
Los efectos del uso masivo del amoniaco en el medio ambiente van más allá de la contaminación del aire, con consecuencias negativas sobre los ecosistemas. Por ejemplo, una gran cantidad de los nutrientes contenidos en los fertilizantes no son utilizados por las plantas y terminan en cuerpos de agua, en donde la disponibilidad de nutrientes puede causar eutroficación y disminución de la biodiversidad.
La producción industrial y masiva de amoniaco a partir del proceso Bosch-Haber representó un desarrollo científico y tecnológico que cambió la historia de la humanidad. Al mismo tiempo, los efectos sanitarios y medioambientales de la liberación antropogénica de amoniaco al medio ambiente han tenido consecuencias negativas para el medio ambiente y la salud humana. En el caso específico del aire, la presencia del amoniaco plantea diversas preguntas que todavía requieren ser estudiadas para entender la magnitud de su impacto y proponer estrategias de mitigación.
La doctora Dara Salcedo González es profesora en la Unidad Multidisciplinaria de Docencia e Investigación de la Facultad de Ciencias, Unidad Juriquilla de la UNAM
AQUI PUEDES LEER TODAS LAS ENTREGAS DE “DESDE LA UNAM”, LA COLUMNA DE LA UNAM, CAMPUS JURIQUILLA, PARA LALUPA.MX
https://lalupa.mx/category/aula-magna/desde-la-unam/